ポイント
- 細胞骨格「微小管」に力学ストレスを加えられる装置を開発
- 微小管が変形するとモータータンパク質による物質輸送速度などが変化することを発見
- 物質輸送の阻害が関与する神経疾患などの病理解明に貢献
概要
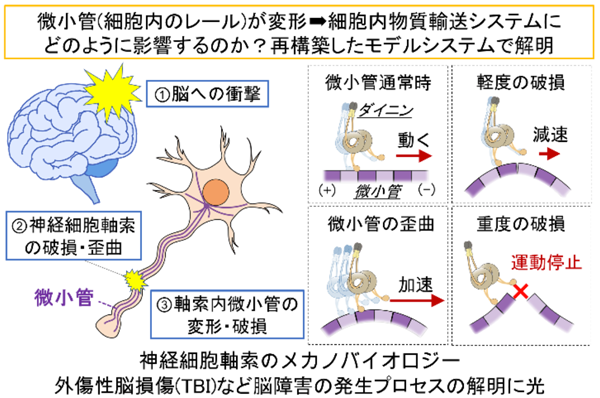
微小変形では輸送速度が増加し、さらに変形すると減速、大変形では微小管が破損し輸送が停止。
背景
研究手法
研究成果
今後への期待
論文情報
用語解説
問合せ先
北海道大学 大学院理学研究院
准教授 角五 彰(かくごあきら)
Tel: 011-706-3474 Fax: 011-706-3474
E-mail:






















国立研究開発法人情報通信研究機構
未来ICT研究所
主管研究員 大岩和弘(おおいわかずひろ)
Tel: 078-969-2112 Fax: 078-969-2119
E-mail:














広報
北海道大学 総務企画部広報課
〒060-0808 札幌市北区北8条西5丁目
Tel: 011-706-2610 Fax: 011-706-2092
E-mail:























国立研究開発法人情報通信研究機構
広報部報道室
〒184-8795 東京都小金井市貫井北町4-2-1
Tel: 042-327-6923 Fax: 042-327-7587
E-mail: